Unit 615, No. 2, Lane 388, Kangan Road, Pudong New Area, Shanghai, China
News Center
NAC-Organ助力RNA疗法新突破:RNA替代蛋白疗法治疗高草酸尿症
原发性高草酸尿症I型(PH1)是一种由于AGXT基因突变导致代谢障碍的罕见遗传性肝病,AGXT基因突变导致肝脏中负责处理乙醛酸的酶活性丧失,草酸在体内过量产生引起肾脏草酸钙结石、肾钙质沉着以及肾功能损伤。当前缺乏根治性治疗方法,临床上主要依赖维生素B6、透析或肝/肾联合移植。
针对PH1开发一种有效、安全且可重复给药的替代疗法,是该领域的重要研究方向。mRNA药物作为一类新兴的治疗手段,在多种遗传病、肿瘤乃中的应用潜力日益受到关注。该疗法中的关键步骤包括序列设计、mRNA合成和生产以及靶向给药。相比于动物模型,人源化体外3D模型能够更精准的模拟人体对药物的反应,能够高通量地筛选、优化mRNA序列,高效地验证递送及治疗效率,极大地提高药物的研发效率。
2025年4月9日,上海交通大学医学院附属仁济医院肝脏外科夏强院士团队在国际知名期刊《Science Advances》(IF=11.7)发表了题为《Preclinical evaluation of AGT mRNA replacement therapy for primary hyperoxaluria type I disease》的最新研究进展。本研究系统评估了基于mRNA的AGT蛋白替代疗法在PH1模型中的表达效率、安全性和治疗效果,构建并应用了包括细胞系、动物模型及患者来源的3D类器官在内的多种体内外实验体系。在该研究中利用朴衡NAC-Organ技术构建的患者及健康人来源的3D肝脏模型,验证了mRNA药物的递送效率,并系统评估了mRNA在体外人源3D模型中的表达特征、定位以及降草酸效果。NAC-Organ技术无需基质胶或水凝胶支撑,可实现mRNA、siRNA、circRNA等药物的自由递送,是高效的药物递送及药效检测工具。本研究中NAC-Organ为新型药物递送系统的开发及治疗方案提供了高度生理相关的功能验证平台,成为推动该项技术向临床转化的关键一环。以下我们为您带来该研究成果的详细解读:

Science Advances,9 Apr 2025
DOI: 10.1126/sciadv.adt96
原文链接:https://www.science.org/doi/10.1126/sciadv.adt9694
研究内容解读
一、hAGT mRNA/ LPP合成及鉴定
研究人员首先通过线性设计算法优化hAGT mRNA的编码序列(CDS)和非翻译区(UTR)。其中2770 hACT mRNA候选序列在HEK293T细胞中表现出更高且更持久的蛋白表达。同样研究人员对于UTR序列也进行了优化,选择了蛋白表达量最高的UTR1进行后续脂质多聚复合物(lipopolyplex,LPP)封装。使用LPP递送mRNA相比于传统脂质纳米颗粒(lipid nanoparticle, LNP)表现出更持久的mRNA表达和有效的肝靶向性(图1)。
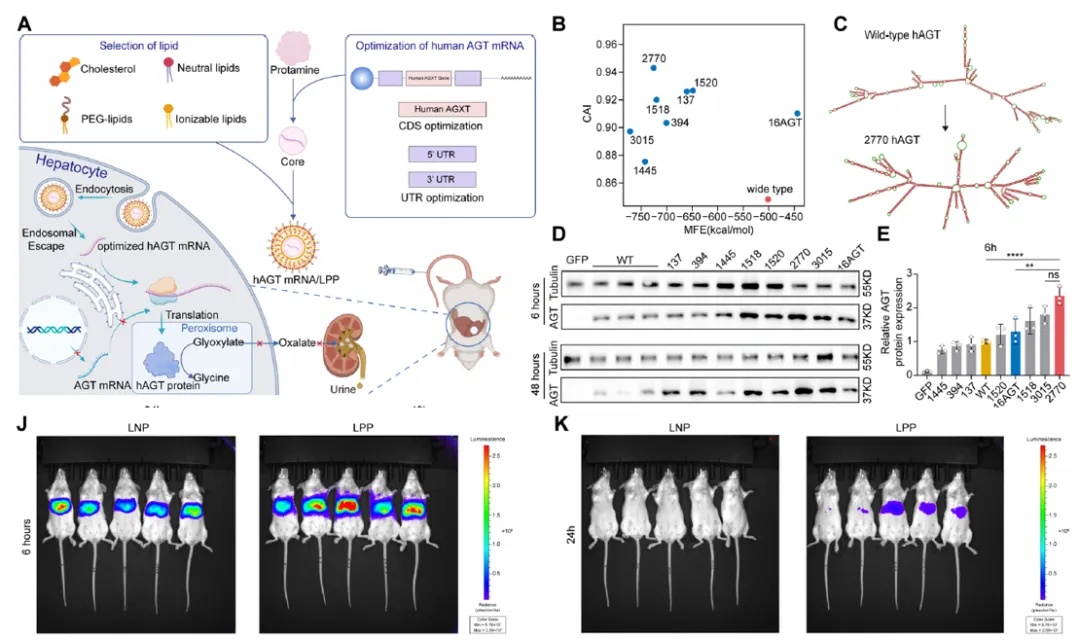
图1. 优化后的hAGT mRNA/ LPP合成及鉴定
二、患者来源3D肝模型验证hAGT mRNA/LPP疗效
传统的2D细胞培养系统单一,难以反映患者的真实病理状态。小鼠等动物模型又常受物种差异以及实验周期及成本的限制。因此在本研究中,研究团队特别选用了人源体外3D模型验证LPP mRNA治疗方法的可行性及效率。研究人员从患有PH1患者的肝脏获得了实质和非实质细胞,利用NAC-Organ技术构建的3D肝脏模型(NAC-Liver)进行了hAGT mRNA/LPP递送以及治疗效果验证。结果表明用hAGT mRNA/LPP的PH1 3D模型中hAGT mRNA显著高表达,转染后的PH1肝3D模型在3天内的草酸盐积累减少了59%。免疫荧光染色表明,PH1肝3D模型中的hAGT蛋白表达水平保持5天。同时hAGT mRNA/LPP转染后在PH1肝3D模型中未观察到明显的细胞损害(图2)。
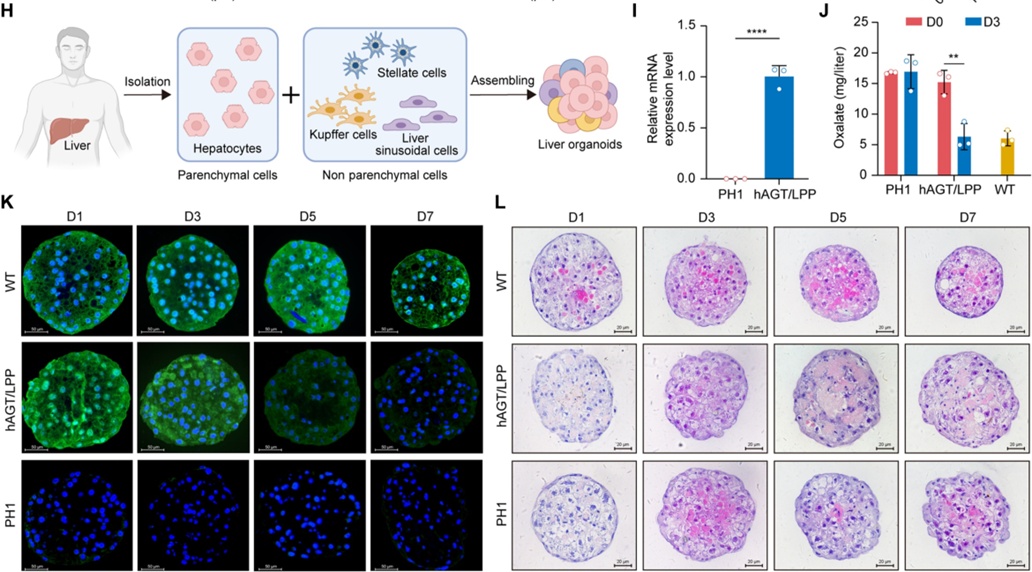
图2. 人3D肝脏模型中hAGT mRNA/LPP作用
三、hAGT mRNA/LPP在野生型小鼠、AgxtQ84−/−大鼠和野生型食蟹猴中的药代动力学
研究人员向野生型(WT)Balb/c小鼠注射了不同剂量hAGT mRNA/LPP用以研究hAGT mRNA 在体内肝脏和血液中以及内源性表达。结果显示各时间点小鼠肝组织中内源性Agxt mRNA 的相对表达差异无统计学意义。给药6小时后人AGT mRNA 的相对表达最高。研究人员向AgxtQ84-/-大鼠注射了不同剂量hAGT mRNA/LPP用以研究hAGT mRNA在肝脏中的表达,该趋势与Balb/c 小鼠肝脏相似。研究人员同样在灵长类动物即食蟹猴上进行了验证。通过静脉注射 hAGT mRNA/LPP,持续 2 周给药后,野生型食蟹猴肝脏中 hAGT mRNA 表达在第 1 次和第 3 次给药后 48 小时较高,第3次给药后144小时仍可检测到mRNA表达。Western blot和免疫组化结果同样验证了hAGT蛋白的持续表达(图3)。

图3. hAGT mRNA/LPP在WT BALB/c小鼠、AgxtQ84−/−大鼠和WT食蟹猴的药代动力学
四、hAGT mRNA/LPP在AgxtQ84−/−小鼠、大鼠体内的药效检测
为了验证hAGT mRNA/LPP在体内发挥的作用,研究人员给予AgxtQ84−/−小鼠单次不同剂量的hAGT mRNA/LPP,并在第0、1、3、5和7天收集24小时尿液样本用于草酸盐检测。在第1天即可观察到尿草酸盐的显着降低,并且持续到第7天尿草酸盐水平一直低于基线值。给予AgxtQ84−/−大鼠单次不同剂量的hAGT mRNA/LPP,并收集不同时间点的尿样。结果显示注射后 72 小时内均草酸盐水平迅速降低,尿草酸盐减少了 57.98%。随后研究人员还对大鼠注射了hAGT mRNA/LPP和维生素B6(一种AGT辅酶)以评估其对AgxtQ84−/−大鼠草酸盐代谢的影响。所有注射组的大鼠血清草酸盐浓度均降低(图4)。
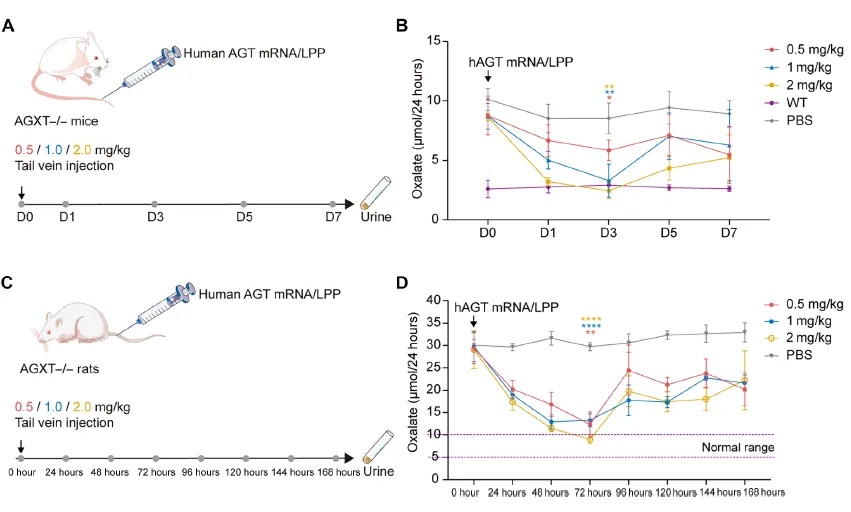
图4. hAGT mRNA/LPP在AgxtQ84−/−小鼠、大鼠体内药效检测
五、系统毒理评估验证安全性
在确认mRNA疗法具有良好药效后,研究团队对其进行了全面的安全性评估。实验涵盖小鼠、大鼠及非人灵长类(食蟹猴)等多个物种,采用重复静脉注射方式,观察多个生理指标的变化。结果表明,hAGT mRNA/LPP在2 mg/kg剂量下无明显严重毒性反应,为该疗法的最高非严重毒性剂量(HNSTD)。在小鼠和大鼠中,虽然高剂量组在体重增长、部分肝酶指标等方面出现一定波动,但均未观察到器官结构损伤或持续性异常反应;炎症因子、免疫指标及组织学检查结果也显示良好的生物相容性(图5)。
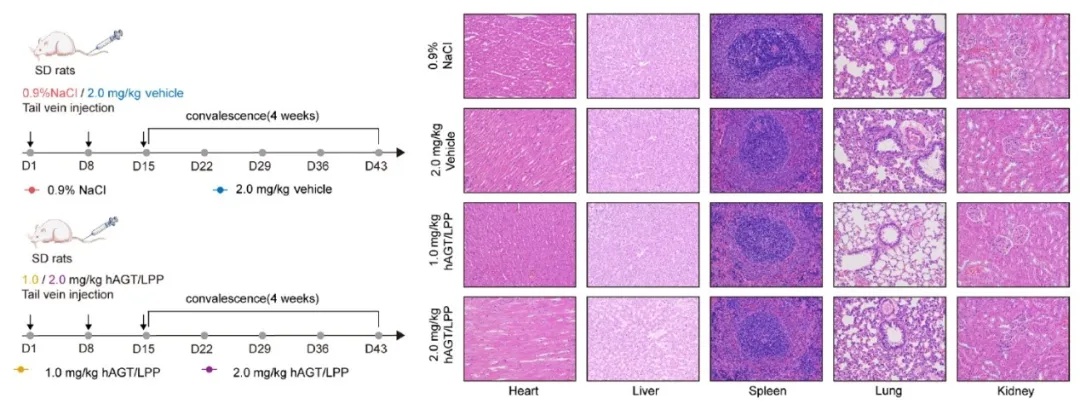
图5. SD大鼠中的hAGT mRNA/LPP毒理学检测
“
总 结
本研究针对遗传性肝病PH1设计并且优化了hAGT mRNA序列组成以及药物递送载体后。随后在细胞、3D模型及动物水平上验证了hAGT mRNA/LPP的递送及表达高效性、持久性。在小鼠、大鼠及非人灵长类(食蟹猴)体内实验中验证了mRNA治疗的药效以及安全性,是遗传性肝病PH1替代性疗法方面的重要突破。
朴衡自主研发的NAC-Organ技术在疾病建模、药效验证与机制研究等方面具有独特优势,在大规模动物或临床前评价体系中极具应用价值。可对新型蛋白、核酸、小分子药物设计、载药方法、递送效率、药物药效进行高通量快速筛选与鉴定。NAC-Organ技术无需基质胶或水凝胶支撑,可实现mRNA、siRNA、circRNA等药物的自由递送,是高效的药物递送及药效检测工具。
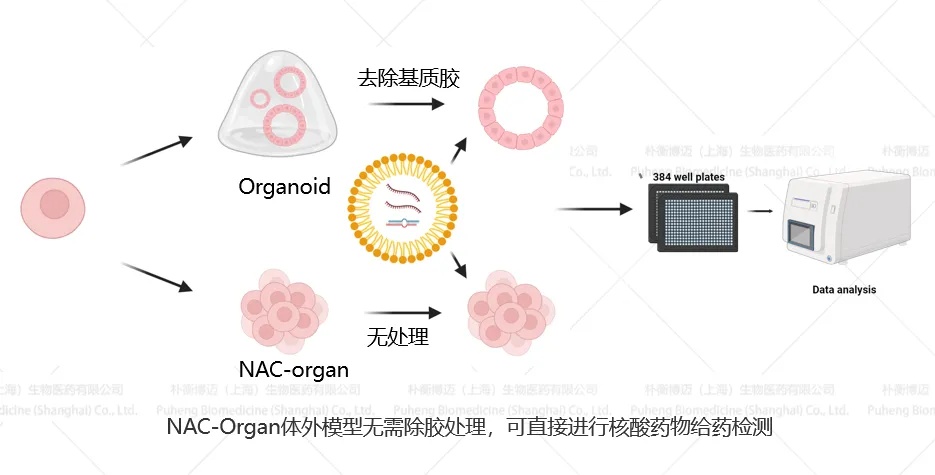
NAC-Organ技术检测mRNA药物优势
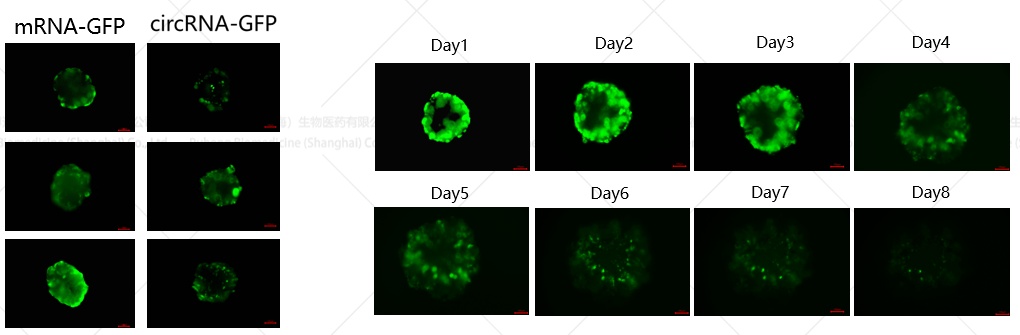
NAC-Organ技术检测RNA药物递送效率及稳定性
- Previous article:朴衡MASH模型助力揭示肝纤维化“关键通路”,GPR91成为潜在治疗新靶点
- next:文献分享 | 基于BMSCs的梯度微环境模拟软骨类器官在骨软骨修复中的研究进展
